論文を読んでいて、ちょっとおかしな点があったので酔った勢いで知り合いに連絡を取って、レターを書いたら、脳卒中の某 top journalに通りました。普段は酔った勢いで失敗してばかりですが、プラスに働くこともあるんですね。あと、編集中の雑誌が出版間際なのですが、原稿落ちの危機にあって 5日間で総説一本書き上げました。普段読んだ論文をブログ記事にしているため、ブログ内検索しながら引用すべき文献を見つけられて、結構楽でした。忙しいけれど、こうして書いておくと、何かの役に立ちますね。
①Effectiveness and safety of reduced dose non–vitamin K antagonist oral anticoagulants and warfarin in patients with atrial fibrillation: propensity weighted nationwide cohort study. (2017.2.1o published online)
腎障害、年齢、体重などにより、NOACは減量して用いる。減量して用いた患者でのコホート研究 (propensity scoreを使用) が BMJ誌に掲載された。その結果、虚血性脳卒中及び全身性塞栓症リスク (%/year) は、アピキサバン 4.8,ダビガトラン 3.3, リバロキサバン 3.5, ワルファリン 3.7だった。ワルファリンとの比較では、効果に関するハザード比は、アピキサバン 1.19 (95%CI 0.95-1.49), ダビガトラン 0.89 (0.77-1.03), リバロキサバン 0.89 (0.69-1.16) だった。主要安全性アウトカムは、アピキサバン 0.96 (0.73-1.27), ダビガトラン 0.80 (0.70-0.92), リバロキサバン 1.06 (0.87-1.29) だった。
通常量だと NOAC間で効果に差がなくアピキサバンの出血リスクが低そうという結果だったが、減量量に関していえば、アピキサバンは効果が劣る、ダビガトランの出血リスクが低いということで、ダビガトランに軍配があがりそうだ。
②Optimal Timing of Anticoagulant Treatment After Intracerebral Hemorrhage in Patients With Atrial Fibrillation. (2016.12.20 published online)
心房細動のある患者が脳出血を発症した場合、いつ頃から抗凝固療法を再開すればよいかを調べたコホート研究。脳出血発症 7~8週間後から再開すると、効果とリスクの比が最もよさそうだ。
③Cardioembolic Stroke. (2017.2.3 published online)
④Atrial Fibrillation and Mechanisms of Stroke: Time for a New Model. (2017.1.19 published online)
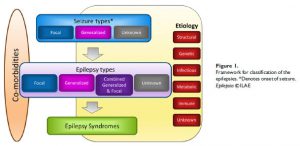
③と④は同じ著者による論文。心房細動では説明できない心原性脳塞栓症が多いことがわかってきていて、心房心筋症や心房の線維化など、心房基質の異常というモデルが注目されているという内容。2017年1月9日のブログ記事で詳しく紹介した論文と似た内容。
⑤Histopathological Differences Between the Anterior and Posterior Brain Arteries as a Function of Aging. (2017.2.14 published online)
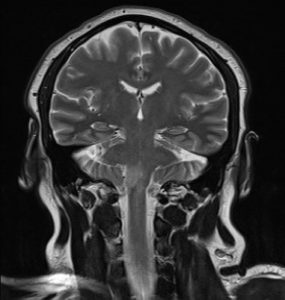
脳バンクの 194剖検脳を用いて、脳の前方循環と後方循環の動脈の病理組織学な違いを検討。後方循環の動脈は前方循環と比べて、壁が薄く、エラスチンが少なく、求心性の内膜肥厚が強かった。前方循環と比べると、脳底動脈は内弾性板に囲まれた動脈の面積が大きく (動脈拡張を示唆する)、椎骨動脈はエラスチンの欠損、求心性内膜肥厚、非アテローム硬化性狭窄が強かった。若者では椎骨動脈の石灰化が前方循環よりも強かったが、加齢とともにこの差は目立たなくなった。
前方循環と後方循環の脳梗塞の違いを比較するときに役に立ちそうな報告だと思う。
⑥Intravenous Thrombolysis in Unknown-Onset Stroke: Results From the Safe Implementation of Treatment in Stroke-International Stroke Thrombolysis Registry. (2017.2.7 published online)
発症時刻不明で血栓溶解療法をおこなった症例と、発症 4.5時間以内に血栓溶解療法をおこなった症例を比較した。その結果、発症時間不明の脳卒中では、発症4.5時間以内とくらべて、症候性出血は増えなかった (調整オッズ比 1.09, 95%CI 0.44-2.67) が、死亡が増え (調整オッズ比 1.58, 95%CI 1.04-2.41)、良好なアウトカム (mRS) は減少した (調整オッズ比 1.29, 95%CI 1.01-1.65)。
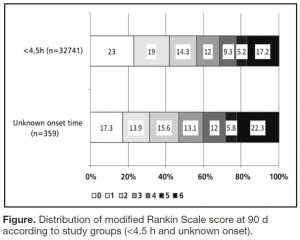
mRS at 90 days
発症時刻不明の脳卒中症例で、頭部CTで early signが出ていなかったり、頭部MRIの拡散強調像での高信号域が狭かったりすると、私は「まだ発症してすぐなんだろうな」と思いながら、血栓溶解療法は結局やらない (というか、基本的に発症 4.5時間以内というのが確認できる症例じゃなきゃ、やっちゃダメだし)。発症時刻不明の脳卒中で血栓溶解療法をすると、発症 4.5時間以内の症例に比べて予後が悪くなるというのは予想できる結果だったけど、どの程度というのがわかって勉強になった。
⑦Association of Preceding Antithrombotic Treatment With Acute Ischemic Stroke Severity and In-Hospital Outcomes Among Patients With Atrial Fibrillation. (2017.3.14 published online)
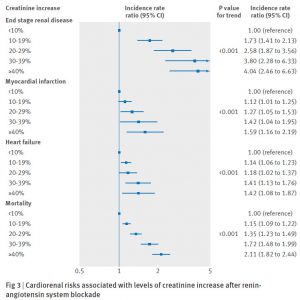
心房細動の既往のある急性期虚血性脳卒中患者 94474名を対象として、発症前におこなわれていた治療と脳卒中の重症度 (NIHSS 16点以上を中等度~重症脳卒中と定義) を後方視的に調べた。脳卒中発症前に 7.6%が治療域 (INR≧2) のワルファリン、8.8%が NOACsを内服していた。83.6%は治療域の抗凝固療法を受けていなかった。13.5%はワルファリンを内服していたが治療域でなく、39.9%は抗血小板薬単独であり、30.3%は何の抗血栓治療も受けていなかった。CHA2DS2-Vasc 2点以上で抗凝固療法をおこなっていなかった理由の内訳は、記載なし 65.8%, 出血リスク 16.3%, 転倒リスク 10.3%, 終末期 6.2%, 患者の拒否 4.3%などだった。交絡因子で調整後、発症前に抗血栓療法がおこなわれていた患者では、中等度~重症脳卒中 (調整後オッズ比 治療域のワルファリン 0.56 [95%CI 0.51-0.60], NOACs 0.65 [0.61-0.71], 抗血小板薬 0.88 [0.84-0.92]) および院内死亡 (調整後オッズ比 ワルファリン 0.75 [0.67-0.85], NOACs 0.75 [0.72-0.88], 抗血小板薬 0.83 [0.78-0.88]) のオッズが低かった。
神経内科医になって、心房細動があるのに抗凝固療法をされずに心原性脳塞栓症で運ばれてくる患者さんを日々みて切々と感じていたのは、「なぜこの方は抗凝固療法をされていなかったのだろう。ひょっとしたら防げていたかもしれないのに。」ということ。おそらく NOACsが発売になり製薬会社がプロモーションの一環として抗凝固療法の必要性の啓蒙活動をするようになったこと、CHADS2あるいは CHA2DS2-Vasc scoreが知られるようになり抗凝固療法の適応がわかりやすくなったことが原因で、最近では適切に抗凝固療法が行われている症例が増えていると思う。そして、きちんと予防治療されている患者では、仮に虚血性脳卒中を発症しても軽くすむことが多いというデータ。抗血小板薬でも中等度~重症脳卒中および院内死亡の低下とこれだけ相関があるというのは少し驚きだった。
⑧Validating the HERDOO2 rule to guide treatment duration for women with unprovoked venousthrombosis: multinational prospective cohort management study. (2017.3.17 published online)
誘因のない静脈血栓塞栓症において、女性の 51.3%が HERDOO2 (Hyperpigmentation, Edema, or Redness in either leg; D-dimer level ≥250 μg/L; Obesity with body mass index ≥30; or Older age, ≥65 years) の low riskに分類された。この場合、5-12ヶ月の短期間で抗凝固療法をやめても再発率は低かった (3.0% per patient year, 95% confidence interval 1.8% to 4.8%)。HERDOO2高リスク女性および男性では、治療を中止すると 8.1% (95%CI 5.2% to 11.9%) per patient yearの再発があり、抗凝固療法を続けた場合は 1.6% (95%CI 1.1-2.3%) per partient yearの再発リスクだった。
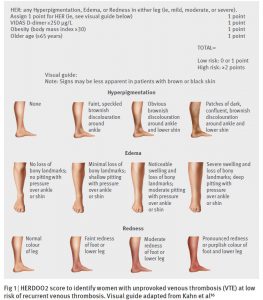
HERDOO2
いつまで抗凝固療法をつづけるかの指標として便利なので覚えておきたい。
⑨Tumefactive demyelination following treatment for relapsing multiple sclerosis with alemtuzumab. (2017.2.8 published online)
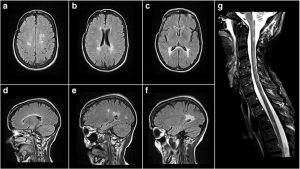
症例は 39歳の女性。24歳時に再発緩解型多発性硬化症と診断。Glatiramer acetate→fingolimod→natalizumabで治療してきて、JC virusが陽性となったことを転機に alemtuzumabに変更。4ヶ月後、脱髄病巣による腫瘤形成がみられた。著者らは、リンパ球の populationが劇的に変化したためではないかと推測している。
Alemtuzumabは、種々の副作用のため米国では承認が延長された過去があり、最近副作用絡みの報告が専門誌に散見されるので、かなり注意して使わないといけない薬剤だと思う。
⑩Treatment effectiveness of alemtuzumab compared with natalizumab, fingolimod, and interferon beta in relapsing-remitting multiple sclerosis: a cohort study. (2017.2.10 published online)
再発寛解型多発性硬化症について、alemtuzumabと他の薬剤を比較したコホート試験。年間再発割合は、alemtuzumab 0.19 vs interferon beta 0.53, alemtuzumab 0.15 vs fingolimod 0.34, alemtuzumab 0.20 vs natalizumab 0.19だった。障害のアウトカムでは、alemtuzumabは interferon beta, fingolimod, natalizumabと比較して有意差はなかった。alemtuzumabは障害の改善において、 interferon beta, fingolimodと差はなく、natalizumabより劣った。
Alemtuzumabや natalizumabの再発抑制効果は高いことはよくわかるけれど、いずれも副作用が気になるところ。重症例向けの薬剤なのだろうな・・・。
⑪Long-term Outcomes After Autologous Hematopoietic Stem Cell Transplantation for Multiple Sclerosis. (2017.2.20 published online)
多発性硬化症に対する自家造血幹細胞移植の長期成績。281名の患者、追跡の中央値 6.6年の報告。78%が進行型の多発性硬化症だった。末梢血幹細胞の mobilizationをしたときの EDSSスコアの中央値は、6.5だった。8名 (2.8%, 95%CI 1.0-4.9%) が移植後 100日以内に死亡した。EDSSスコアによる評価で悪化がなく 5年間過ごせたのは 46%だった。移植後の神経学的疾患進行に関する因子は、高齢、進行型、2種類以上の疾患修飾薬を使用した既往であった。ベースラインの EDSSスコアが高い患者では、全生存の悪化と関連があった。
移植治療は侵襲の大きな治療で、約3%が移植に関連して亡くなるが、うまくいけば約半数の患者で明らかな進行なく過ごせるという、ハイリスク・ハイリターンの治療。
⑫Neurodegeneration in multiple sclerosis and neuromyelitis optica. (2016.9.28 published online)
多発性硬化症と視神経脊髄炎の神経変性についての総説。多発性硬化症では髄鞘が障害されやすいけれど、視神経脊髄炎では軸索が障害されやすいことを説明した図がわかりやすい。
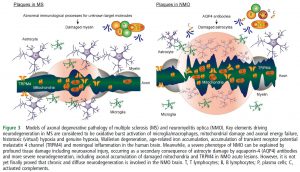
MS and NMO
⑬Possible liver injury added to label of Biogen MS drug (2017.1.25)
2017年2月22日に本邦でも発売開始となった フマル酸ジメチル (商品名 テクフィデラ) だが、米国では 添付文書に肝障害の副作用について記すことになったらしい。フマル酸ジメチルで重度の肝障害をきたした症例が複数報告されており、販売するバイオジェンのスポークスマンによれば、23万人治療して、14例だったとのこと。発症時期は数日~数ヶ月で幅があるらしい。
最近の医学論文【中】